cytidine hører til nukleosidene og består av nukleicbase cytosin og sukker ribose. Det danner et basepar med guanosin via hydrogenbindinger. Det spiller også en sentral rolle i pyrimidinmetabolismen.
Hva er cytidin?
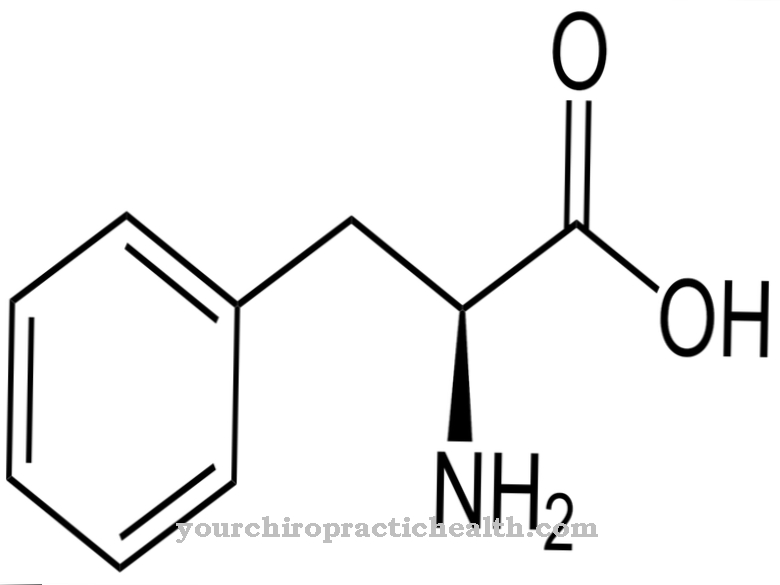
Cytidin er et nukleosid som består av cytosin og ribose. I tillegg til adenin, guanin og timin, er nitrogenbase-cytosin involvert i syntesen av nukleinsyrer. Fosforylering av cytidin produserer cytidinmonofosfat (CMP), cytidindifosfat (CDP) eller cytidintrifosfat (CTP).
Cytidinmonofosfat er et nukleotid i RNA. To purin- og to pyrimidinbaser er involvert i strukturen til nukleinsyrene, hvor tymin byttes ut mot uracil i RNA. Adenin og guanin tilhører purinbaseene, mens tymin, cytosin og uracil tilhører pyrimidinbaseene. Cytidindeaminase kan deaminere cytidin til uridin. Uridine er et nukleosid laget av ribose og uracil. Det kan også fosforyleres til uridinmonofosfat.
Uridin monofosfat er også et viktig nukleotid for RNA. Videre er CDP og CTP også aktiverende grupper for syntese av lecithin, cephalin og cardiolipin. Det rene cytidinet er til stede som et vannløselig fast stoff som spaltes ved 201 til 220 grader. Det kan bli katalytisk nedbrutt til cytosin og ribose av enzymet pyrimidin nucleosidase.
Funksjon, effekt og oppgaver
Cytidin spiller en sentral rolle i pyrimidinmetabolismen. Pyrimidin gir den grunnleggende strukturen for pyrimidinbasene cytosin, timin og uracil som forekommer i nukleinsyrer. Thymin i RNA byttes mot uracil.
Uracil produseres også ved deaminering av cytidin og cytidindeaminase. De kjemiske omdannelsene mellom de tre pyrimidinbasene er av sentral betydning for reparasjonsprosessene i DNA og de epigenetiske endringene. I sammenheng med epigenetikk blir forskjellige egenskaper modifisert av miljøpåvirkninger. Arvestoffet endrer seg imidlertid ikke. Modifikasjonsendringer av en organisme er forårsaket av forskjellige uttrykk for gener. Differensieringsprosesser av kroppens celler for dannelse av forskjellige cellelinjer og organer representerer også en epigenetisk prosess.Avhengig av celletypen, aktiveres eller deaktiveres forskjellige gener.
Dette skjer gjennom metylering av cytidinbasene i DNA. Under metylering dannes metylcytosin som kan omdannes til timin ved deaminering. Den komplementære nukleobase-guaninen i den motsatte dobbeltstrengen gjør det mulig å gjenkjenne feilen og tymin kan byttes ut mot cytosin igjen. Imidlertid kan guanin også byttes mot adenin, noe som fører til en punktmutasjon. Hvis det ikke-metylerte cytosinet blir deaminert, produseres uracil. Siden uracil ikke vises i DNA, erstattes det øyeblikkelig med cytosin. I stedet for cytosin økes mutasjonshastigheten på grunn av metylering litt.
Samtidig blir flere og flere gener slått av gjennom metylering, slik at cellene i cellelinjen blir mer spesialiserte. I reparasjonsprosesser er reparasjonsenzymer basert på den opprinnelige DNA-strengen, som de gjenkjenner gjennom en høyere grad av metylering. Den komplementære strengen er også bygget på grunnlag av informasjonen som er lagret der. Installasjonsfeil blir rettet umiddelbart. Videre katalyserer enzymet AID (Activation Induced Cytidin Deaminase) veldig spesifikt deaminasjonen av cytidingrupper til uridingrupper i enstrenget DNA. Somatiske hypermutasjoner forekommer, som endrer antistoffsekvensene til B-celler. Deretter blir de matchende B-cellene valgt. Dette muliggjør en fleksibel immunrespons.
Utdanning, forekomst, egenskaper og optimale verdier
Cytidin er et mellomprodukt av pyrimidinmetabolismen. Som en isolert forbindelse spiller det ingen rolle. Som allerede nevnt er det sammensatt av nukleisk base cytosin og kvintuple sukker ribose. Kroppen kan syntetisere cytosin selv.
Syntesen er imidlertid veldig energikrevende, slik at den utvinnes fra byggesteiner for nukleinsyre innenfor rammen av bergingsveien og kan integreres i nukleinsyrer. Når basen er helt nedbrutt produseres karbondioksid, vann og urea. Det er til stede som et nukleosid i RNA. I DNAet er cytosin bundet til deoksyribose, slik at nukleosiddeoksycytidinet forekommer her som en byggestein.
Sykdommer og lidelser
Metyleringene på cytidinrestene av DNA er veldig viktige for markeringer for å skille forskjellige biokjemiske prosesser. Imidlertid kan det også oppstå feil i metylering som fører til sykdom.
Ved mangelfulle metyleringer kan både økt og redusert genaktivitet utløses som ikke tilfredsstiller kravene. Disse metyleringsmønstrene blir gitt videre under celledeling. På lang sikt skjer det endringer som kan føre til sykdommer. Noen tumorceller har for eksempel forskjellige metyleringstrukturer som ikke forekommer i friske celler. For eksempel kan metylering blokkere visse gener som koder for vekstregulerende enzymer. Hvis disse enzymene mangler, kan uhemmet cellevekst oppstå. Dette gjelder også enzymer som initierer ordnet celledød (apoptose) når celledefekter oppstår.
En målrettet påvirkning av DNA-metylering er ennå ikke mulig. Imidlertid er det studier på fullstendig demetylering av tumorceller for å underlegge dem igjen for kontroll av de vekstregulerende proteiner. I følge flere kliniske studier er det vist at demetylering begrenser tumorvekst hos pasienter med akutt myelooid leukemi. Denne prosedyren er også kjent som epigenetisk terapi. Metyleringsprosesser kan også spille en rolle i andre sykdommer. På grunn av miljømessige påvirkninger tilpasser organismen seg til endrede forhold med dannelse av biologiske modifikasjoner basert på metyleringer av cytidinrester av DNA. Kroppen gjennomfører dermed en læringsprosess, som imidlertid også kan forårsake feil regulering.

.jpg)

.jpg)




.jpg)